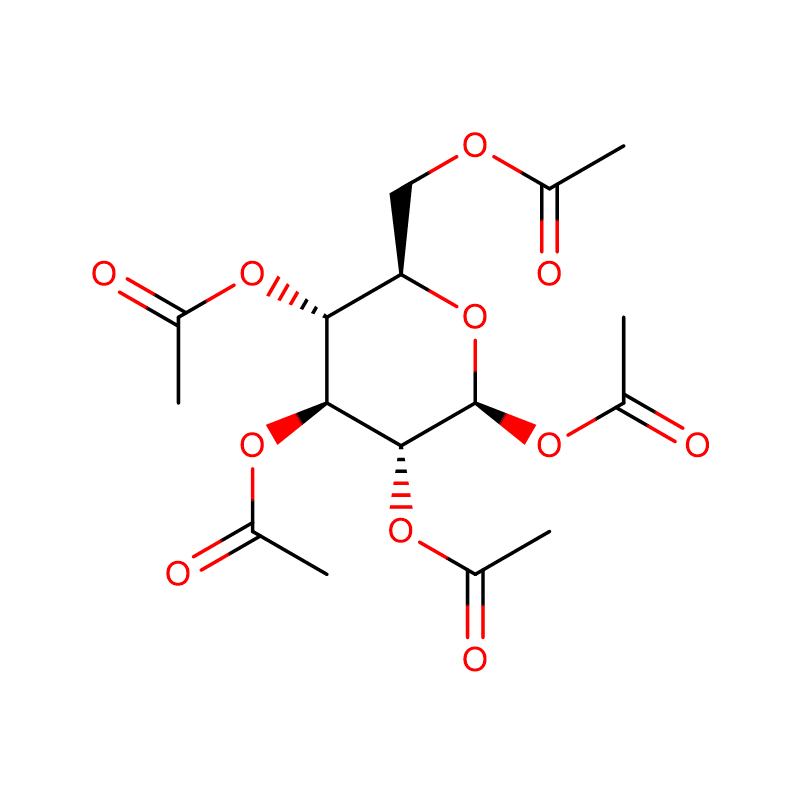
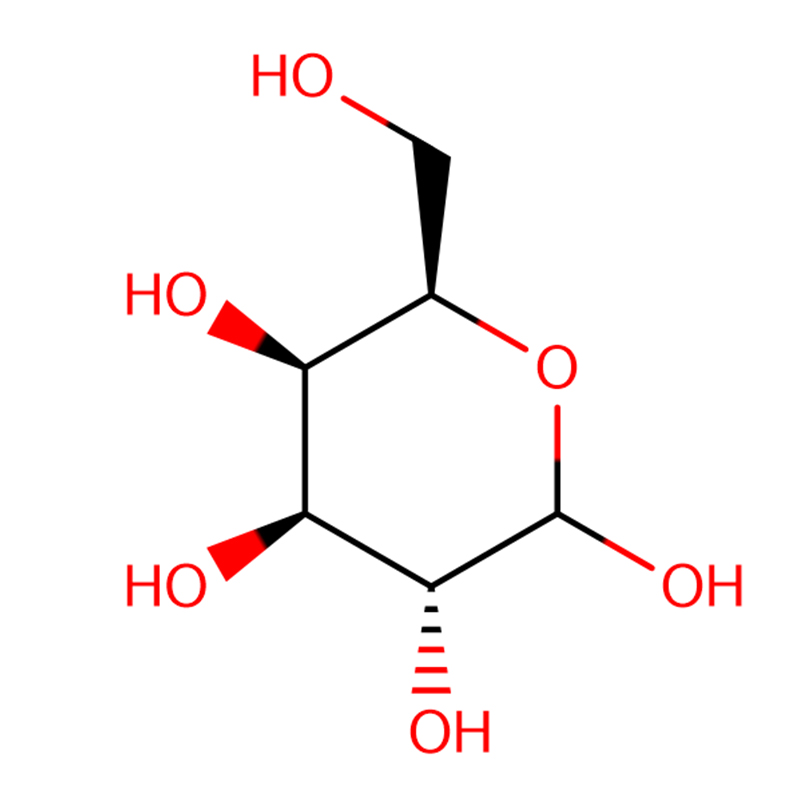
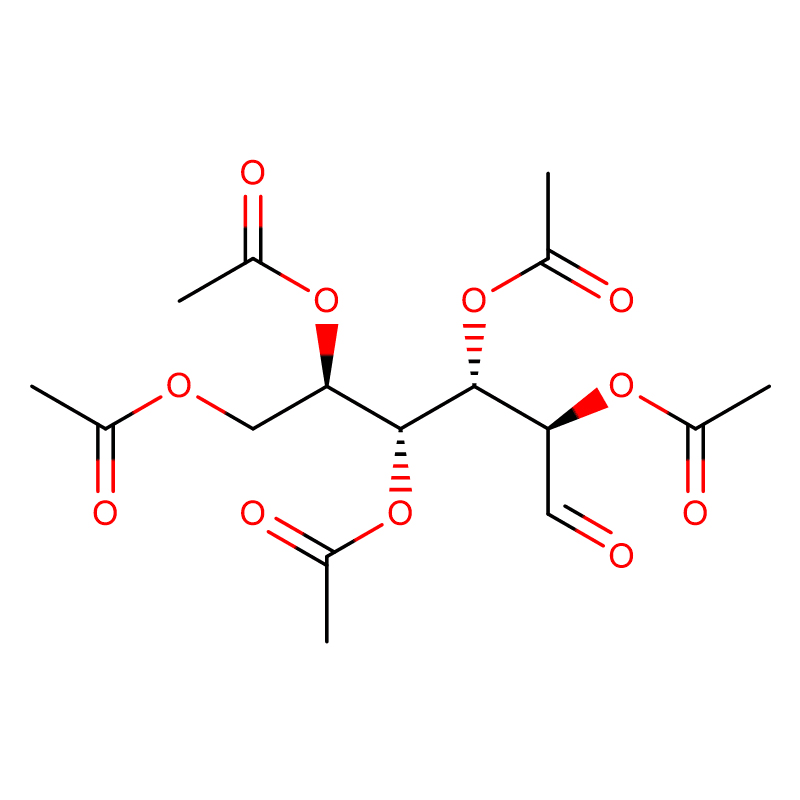
4-НИТРОФЕНИЛ-АЛФА-Д-МАНОПИРАНОЗИД CAS:10357-27-4 бел прав 98%
| Број на каталог | XD90011 |
| Име на производ | 4-Нитрофенил-алфа-D-манопиранозид |
| CAS | 10357-27-4 |
| Молекуларна формула | C12H15NO8 |
| Молекуларна тежина | 30301.25 |
| Детали за складирање | -2до -8°C |
| Усогласен тарифен код | 29400000 |
Спецификација на производот
| Вода | <5% Карл Фише |
| Растворливост | 1% во DMF е бистар и безбоен |
| Чистота | Бесплатен 4-нитрофенол <200 ppm |
| HPLC | > 98% |
| Изглед | Прашок со бела боја |
Механистички увиди во фамилија на алфа-манозидази зависни од Ca2+ во човечки цревни симбионти.
Бактериите на колонот, примерот на Bacteroides thetaiotaomicron, играат клучна улога во одржувањето на човековото здравје со искористување на големи семејства на гликозидни хидролази (GHs) за да се искористат диеталните полисахариди и гликаните домаќини како хранливи материи.Таквото проширување на семејството на GH е пример за 23 фамилија GH92 гликозидази кодирани од геномот B. thetaiotaomicron.Овде покажуваме дека ова се алфа-манозидази кои дејствуваат преку еден механизам за поместување за да користат N-гликани на домаќинот.Тридимензионалната структура на две GH92 манозидази дефинира семејство на протеини со два домени во кои каталитичкиот центар се наоѓа на интерфејсот на доменот, обезбедувајќи киселински (глутамат) и базен (аспартат) помош за хидролиза во Ca(2+)- зависен начин.Тридимензионалните структури на GH92 во комплекс со инхибитори обезбедуваат увид во специфичноста, механизмот и конформациската маршрута на катализата.Ca(2+) игра клучна каталитичка улога во помагањето да се изобличи манозидот од неговата конформација на столот (4)C(1) кон преодната состојба. (Библиографија: Нац.Chem.Биол.6, 125-32, (2010)
Фронтална афинитетна хроматографија на овалбумински гликоаспарагини на колона конканавалин А-сефароза.Квантитативна студија за специфичноста на врзувањето на лектинот.
Интеракциите на Sepharose 4B-имобилизираниот конканавалин А (ConA) со 10 гликоаспарагини добиени од овалбумин беа квантитативно истражени со фронтален афинитетен хроматографија.Во овој метод, раствор од јаглени хидрати се нанесува континуирано на колона ConA-Sepharose и ретардацијата на предниот дел на елуцијата се мери како параметар на јачината на интеракцијата.Може да се одреди константата на дисоцијација (Kd) за секој сахарид со ConA.Анализата на врзувањето на р-нитрофенил-алфа, Д-манозид покажа дека врзувачките својства на ConA не се менуваат суштински по имобилизацијата на Sepharose 4B.Секој од овалбуминските гликоаспарагини беше означен со тритиум со методот на редуктивна метилација за анализа.Споредбата на добиените вредности на Kd покажа дека врзувањето на ConA значително варира со многу мали структурни разлики на синџирот на гликозил.Резултатите сугерираат дека ConA препознава специфична структура на гликозилен синџир, Man alpha 1-6(Man alpha 1-3)Man, во која најмалку една хидроксилна група на позицијата C-3 на C-6-поврзана маноза треба да биде слободна.