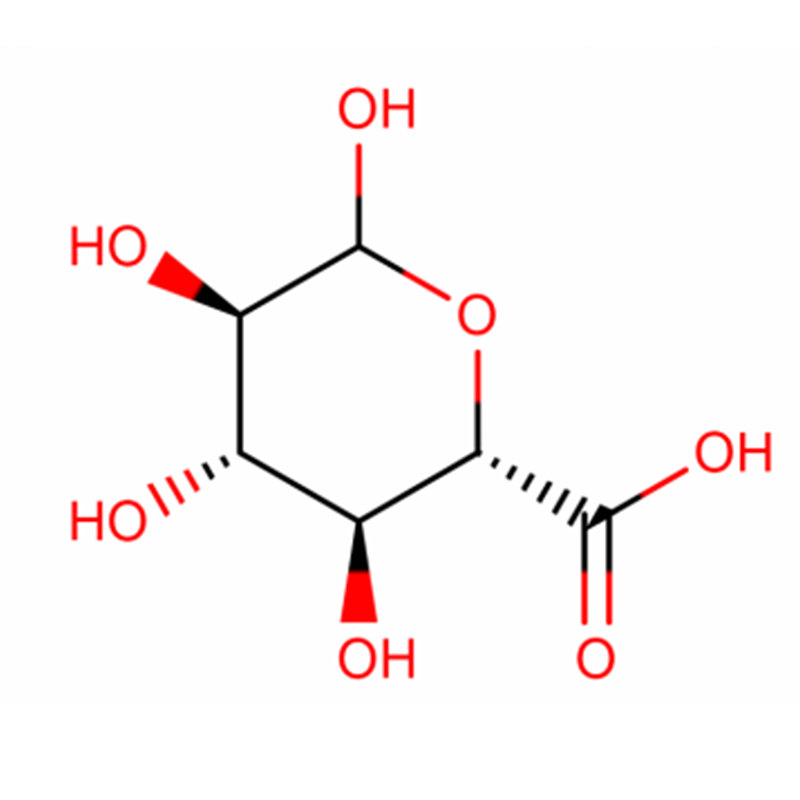
Биосинтезата на протеогликаните и гликозаминогликаните во присуство на р-нитрофенил-ксилозид беше проучена со користење на систем за клеточна култура на примарен оваријален гранулоза на стаорец.Додавањето на р-нитрофенил-ксилозид во медиумот за клеточна култура предизвика околу 700% зголемување на инкорпорацијата на [35S]сулфат (ED50 на 0,03 mM) во макромолекулите, кои вклучуваат слободни синџири на хондроитин сулфат иницирани на ксилозид и природни протеогликани.Слободните синџири на хондроитин сулфат иницирани на ксилозид беа речиси исклучиво секретирани во медиумот.Молекуларната големина на синџирите на хондроитин сулфат се намали од 40.000 на 21.000 како што беше зголемено вкупното инкорпорирање на [35S]сулфат, што сугерира дека подобрената синтеза на хондроитин сулфат го нарушува нормалниот механизам на завршување на синџирот на гликозаминогликаните.Биосинтезата на протеогликаните на хепаран сулфат беше намалена за приближно 50%, најверојатно поради конкуренцијата на ниво на прекурсори на UDP-шеќер.[35S] Инкорпорацијата на сулфатот беше затворена со додавање на циклохексимид со почетно полувреме од приближно 2 часа во присуство на ксилозид, додека тоа во отсуство на ксилозид беше околу 20 мин.Разликата веројатно ја одразува стапката на обрт на капацитетот за синтеза на гликозаминогликан како целина.Стапката на обрт на синтетизирачкиот капацитет на гликозаминогликан забележана во клетките на гранулозата на јајниците беше многу пократка од онаа забележана кај хондроцитите, што ја одразува релативната доминација на биосинтетичката активност на протеогликанот во вкупната метаболичка активност на клетките.